免疫原性细胞死亡(ICD)将垂死的癌细胞转化为治疗性疫苗,并刺激抗肿瘤免疫反应。在这里,我们揭示了无偏倚的筛查结果,该筛查确定了高剂量(10 μM)的克唑替尼(crizotinib)是诱导ICD的酪氨酸激酶抑制剂,当与非ICD诱导的化学疗法(如顺铂)结合使用时,具有卓越的抗肿瘤活性。顺铂和高剂量克唑替尼的组合可在非小细胞肺癌(NSCLC)细胞中诱导ICD,并有效控制不同的(可移植的,致癌物或致癌基因诱导的)原位NSCLC模型的生长。这些抗癌作用与T淋巴细胞浸润的增加有关,并被T细胞耗竭或干扰素-γ中和所消除。克唑替尼加顺铂可导致肿瘤中PD-1和PD-L1的表达增加,加上NSCLC对PD-1抗体进行免疫治疗的强烈敏感性。因此,常规疗法与克唑替尼一起进行的序贯联合治疗,然后进行免疫检查点阻断,可能对NSCLC有效。
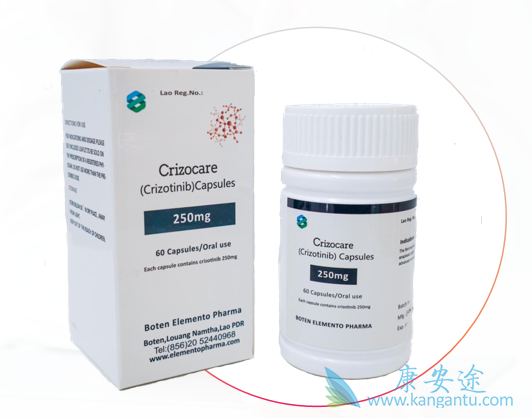
几种可药物致癌基因是酪氨酸激酶,由于突变或基因扩增而被激活。因此,已经开发了针对此类酪氨酸激酶的小抑制分子和抗体(当它们在细胞表面表达时),并已引入临床。确实,针对癌基因的酪氨酸激酶抑制剂(TKI),例如cABL(在费城染色体阳性的慢性髓性白血病,CML中被激活),BRAF(在黑素瘤中被激活),ERBB2(在部分乳腺癌中被激活),EGFR(在非小细胞肺癌的相当大的部分,非小细胞肺癌)活化,KIT(在胃肠道间质瘤中激活)(GIST)或VGFR(在肾癌等中激活)已被批准用于癌症患者的常规治疗。
抗肿瘤TKIs的发展很大程度上受到细胞自主观点的驱动,即:(i)癌症是遗传和表观遗传的细胞疾病;(ii)抗癌药物应针对转化细胞的特定特征,以消除它们或减少其生长。然而,与这一愿景相矛盾的是,伊马替尼甲磺酸盐,这是第一个被引入常规实践的TKI,最初用于治疗CML(如果对ABL激活易位或KIT的激活突变呈阳性),后来对表达GIST的已激活的TKI进行治疗。事实证明,KIT通过刺激NK和T细胞介导的抗癌免疫反应来介导(部分)作用。事实上,在治疗GIST,NK细胞活化和NK细胞活化受体的同种型的表达模式的迹象构成了预测治疗的长期结果超出其停止准确的生物标志物。因此,伊马替尼举例说明了TKI,它除了对恶性细胞有直接作用外,还可能通过抑制树突状细胞(DC)表达的未突变KIT来刺激细胞免疫系统。伊马替尼的成功以及靶向ABL和KIT的第二代TKI的成功在多大程度上可归因于直接作用和免疫依赖性作用,这的确是一个争论的话题。。重要的是,其他TKI也已显示出刺激抗癌免疫反应的能力,因为它适用于索拉非尼和依鲁替尼以及其他。
像蒽环类抗生素,奥沙利铂,紫杉烷类,和环磷酰胺化疗剂也通过间接免疫-依赖性机制已知的它们的抗癌作用居间部分。这些cytotoxicants可能会导致前面有细胞死亡生前应激反应,从而使癌细胞对发射使得它们对免疫系统的检测信号。这种“免疫原性细胞死亡”(ICD)的特征是自噬反应,使细胞在凋亡的起泡阶段或坏死过程中释放ATP。以及内质网(ER)应激反应(以eIF2α的磷酸化为显着特征)导致钙网蛋白(CALR)暴露在细胞表面。ATP充当表达嘌呤能受体的DC前体的趋化因子,而CALR充当“进食”信号,以促进DC对垂死的癌细胞部分(与肿瘤相关抗原)的吞噬作用。
细胞死亡还与细胞质蛋白膜联蛋白A1(ANXA1,其作为甲酰肽受体-1 FPR1的趋化因子,以确保DC与垂死细胞形成突触)的释放有关。核蛋白高迁移率族盒1(HMGB1,通过激活Toll样受体4(TLR4)作为DC成熟因子)。已获得支持ICD以及上述每个配体和受体的重要性的临床证据,这意味着缺乏ICD功能的恶性细胞(例如自噬,CALR和HMGB1)或FPR1或TLR4缺陷的宿主的机会减少化疗后无进展或总体生存的情况。现在克唑替尼的价格是多少?更多详情可咨询下方微信。













请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)