即使更大的竞争使丙型肝炎病毒(HCV)药物价格从平庸平静层次下降(至少有一些),一些制药公司仍然热衷于追求更先进的HCV治疗方法,这可能有助于进一步利用这个仍然有利可图的市场。
目前的优选治疗方法已经非常有效,其治愈率通常在95%至99%的范围内,并且通常是安全和耐受性良好的。但是,与病毒感染的三个主要亚组可能会有今天可用的治疗方案治愈的机会较少:以前用干扰素治疗的hep C方案治疗不成功的肝硬化患者,失代偿性肝硬化患者和肝癌基因型3的患者C型 - 特别是肝硬化。还有没有特别批准的肝癌治疗的亚组。
吉四代Vosevi
此外,研究人员一直在寻求减少治愈HCV所需的治疗时间,至少为更多的人提供了仅需8周治疗的机会,正如许多基因型1的hep C目前可以与吉利德科学的大片Harvoni (ledipasvir /索非布韦)。
吉利德
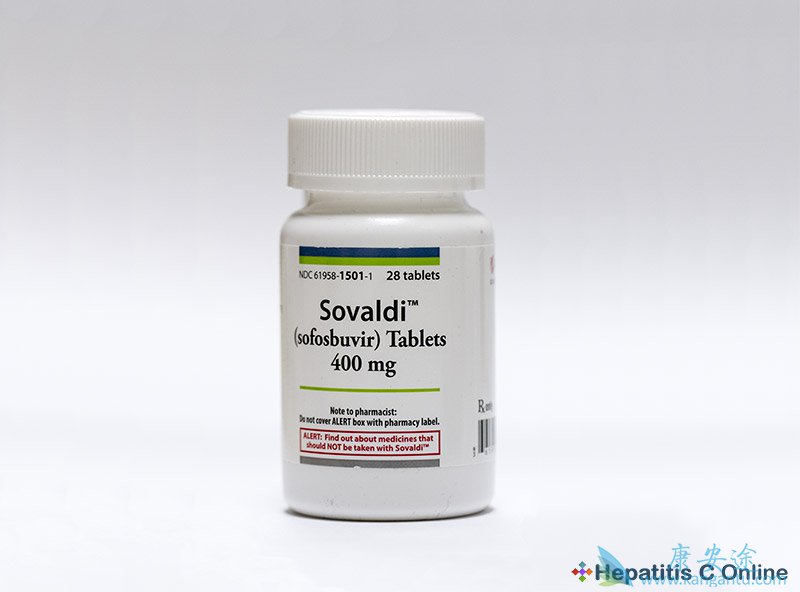
由于吉列在2013年12月发布了NS5B聚合酶抑制剂Sovaldi(sofosbuvir),该公司已经主导了C C市场。
吉四代Vosevi
吉利德随后与Sovaldi配对了另外两种药物,以创建两种新的单一片剂联合HCV方案。将NS5A抑制剂的尿嘧啶添加到Sovaldi中,创造了2014年发布的Harvoni,并被批准用于治疗具有hepC基因型1,4,5和6的那些。接下来,结合pangenotypic(意味着它对HCV的所有基因型进行操作)NS5A抑制剂velpatasvir与Sovaldi产生Epclusa(sofosbuvir / velpatasvir),一种在2016年绿色照明的方案。与以前的两次吉拉德治疗不同,Epclusa被批准用于具有所有基因型(1至6)的C型肝炎。它被批准用于或没有肝硬化,包括先进的疾病形式,失代偿性肝硬化。

最近,吉利德已经将抗生素NS3 / 4A抑制剂维生素维生素添加到了Epclusa的组分中,以进一步改善该治疗。2016年12月,该公司向具有所有基因型病毒(包括没有肝硬化或补偿性肝硬化)的患者申请美国食品和药物管理局(FDA)批准了一项为期12周的sofosbuvir / velpatasvir / voxilaprevir方案以前用直接作用的抗病毒药物(DAAs)治疗。
吉四代Vosevi
目前该药物已经被批准,三联药物组合片剂将是第一次每日一次的单一片剂治疗方案,用于那些以前的DAA治疗失败者。
FDA批准三联组合片剂是一种突破性治疗标准,用于治疗HCV C基因型1的患者,该患者在以前的NS5A抑制剂类别中含有DAA的方案失败。这项指定是针对可能比目前批准的严重疾病治疗提供显着改善的治疗,并加快治疗的批准过程。有关该方案的决定预计将在8月初。

三联组合的FDA应用程序是基于POLARIS试验的数据,包括III期POLARIS-1和POLARIS-4试验,每个试验在以前治疗过的hep C基因型1至6的人群中测试了12周的方案包括那些服用NS5A抑制剂的DAAs。97%的参与者在完成治疗后12周达到持续的病毒学反应(SVR12,被认为是治愈)。
还支持新的药物应用是第三阶段POLARIS-2和-3研究,其中包括肝硬化患者和测试八周的三联药物治疗的首要时间。这些研究发现治愈率达95%至96%。
吉四代Vosevi
艾伯维
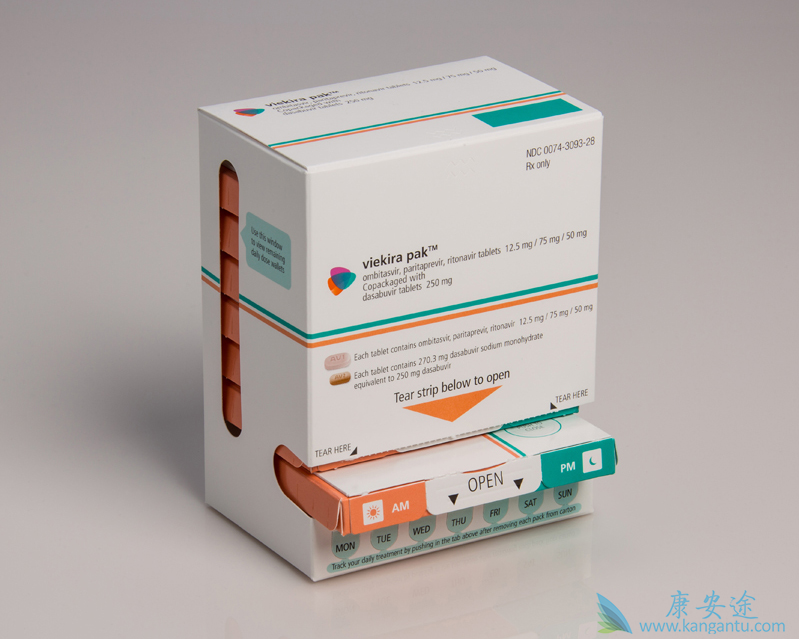
AbbVie目前生产于2014年获得批准的Viekira Pak(ombitasvir / paritaprevir / ritonavir; dasabuvir);Viekira XR(Viekira Pak具有相同的成分,但配方更简单),于2016年通过;和Technivie(ombitasvir / paritaprevir /利托那韦),这些药物的组分包括NS5A抑制剂ombitasvir,NS3 / 4A蛋白酶抑制剂比他他巴,HIV蛋白酶抑制剂Norvir(利托那韦),用于提高其他药物和非核苷NS5B聚合酶抑制剂达沙布韦。
2月份,FDA向AbbVie的新药申请优先审查了NS3 / 4A蛋白酶抑制剂glecaprevir和NS5A抑制剂pibrentasvir(称为G / P)的固定剂量组合片剂。FDA的治疗决定可能会在6月底进行。
美国食品和药品管理局(FDA)将优先审查(将10至6个月的时间缩短)用于严重疾病的治疗,这些疾病可能比目前可用的治疗方法具有安全性或功效优势。
与AbbVie当前批准的方案不同,G / P是pangenotypic。另外,不需要至少12周的治疗,新方案可以获得八周的处方批准,特别是那些没有接受过hep C治疗的那些没有肝硬化的患者。
新药申请基于8项临床试验,共2,300名参与者具有所有HCV基因型,包括慢性肾脏疾病患者。这些试验的最近结果非常有希望,通常具有95%或更高的治愈率和良好的耐受性。
在这些试验中,对于具有基因型1,没有肝硬化并且是治疗的首选者的III期CERTAIN-1研究显示出99%的治愈率;对以前治疗失败的基因型1患者进行第二期MAGELLAN-1研究;对于基因型3的患者,对于12或16周G / P的II期SURVEYOR-II试验;以及没有肝硬化的基因型4,5和6的III期耐受性试验。
最近的一期研究还发现,G / P可以安全地与HIV抗逆转录病毒(ARV)方案Genvoya(埃维埃伐他汀/同型异构氨酸/恩曲他滨/替诺福韦甲酰胺)和Triumeq(dolutegravir /阿巴卡韦/拉米夫定)一起使用,并且不需要剂量调整。
扬森
Janssen市场上唯一的hep C药物是Olysio(simeprevir),于2013年获得批准,必须与Sovaldi(2014年批准配对)结合使用。特别是哈罗尼特别留下来,奥利西奥本身并没有找到一个重要的利基。扬森仍然在发展先进的联合疗法。
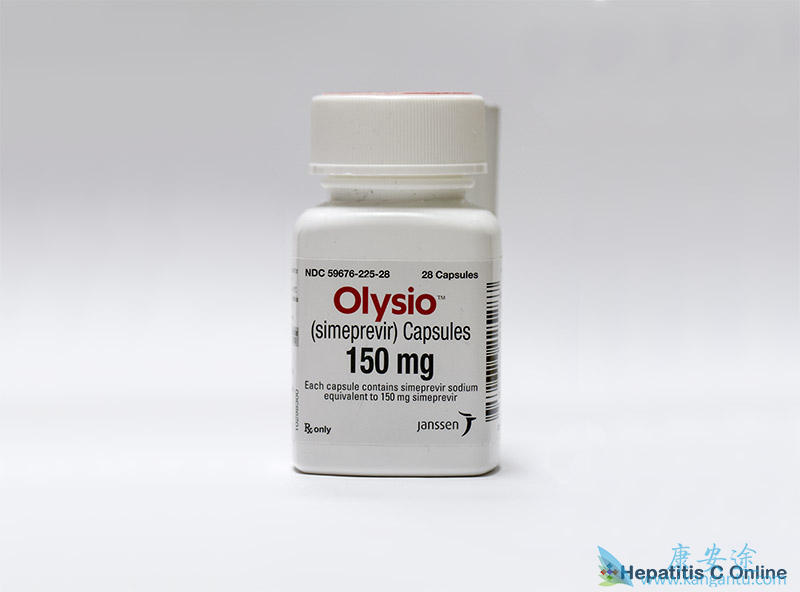
2015年,扬森宣布与Achillion合作开发HCV疗法,重点关注称为JNJ-4178的三联药物治疗,其中包括Olysio,NS5A抑制剂odalasvir和NS5B聚合酶抑制剂AL-335。
JNJ-4178方案的IIb期试验正在对没有肝硬化的基因型1,2,4,5和6基因型的患者进行6周和8周的疗程,其中有些已经接受治疗。
此外,IIa期II期试验目前正在调查六或八周的odalasvir和AL-335,其中有或没有Olysio在基因型1,2和3之间,之前没有接受过治疗,其中一些患有肝硬化。去年秋季发表的临时结果显示,基因型1的患者没有肝硬化。
在制药公司可以申请FDA批准前,调查治疗必须完成III期临床试验。
默克
默克唯一的hepC治疗是Zepatier(elbasvir / grazoprevir),其包括NS5A抑制剂elbasvir(50mg)和NS3 / 4A蛋白酶抑制剂格列唑霉。Zepatier于2016年获得批准,以治疗C型基因型1和4的患者,包括肝硬化患者。

默克目前在II期临床试验中有两种方案。像詹森一样,默克在吉利德和阿维夫的背后进行了新的治疗。
一种方案称为MK-3682B或简称MK-3,其中包括格列保宁,NS5A抑制剂ruzasvir和HCV NS5B抑制剂uprifosbuvir(以前称为MK-3682)。C-CREST 1和2研究的B部分给予8周,12或16周的MK-3给具有hep C基因型1,2和3的那些,其中一些患有肝硬化(其中一些具有基因型2或3的那些接受利巴韦林)。治愈率大概在95%到99%之间。在C-CREST 1和2研究的C部分中,16周的MK-3加利巴韦林治愈了几乎所有那些以前用其他默克治疗方法治愈失败的人。
默克公司还在第二阶段试验中对利福西韦和利扎韦韦加利巴韦林进行双重药物治疗12周治疗,其中包括所有基因型HCV治疗的患者,包括肝硬化患者和艾滋病毒感染者。
施贵宝
BMS生产Daklinza(daclatasvir),一种在2015年批准的NS5A抑制剂,像Olysio一样,必须与Sovaldi结合使用。Daklinza / Sovaldi组合被批准用于hepC基因型1和3的人。

该公司已经退出了HCV药物开发游戏。
















请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)