在治疗周期 1 的维奈托克(venetoclax)加速期(4 天)期间,患者因肿瘤溶解综合征 (TLS) 评估和预防而住院,直到达到维奈托克目标剂量后 24 小时。TLS 的预防包括降尿酸药物和口服或静脉补液。维奈托克与食物一起口服给药,每天一次。维奈托克剂量从第 1 天 100 毫克开始,并在 4 天内逐步增加以达到 600 毫克(100、200、400 和 600 毫克)的目标剂量;从第 4 天到第 28 天继续以每天 600 mg 给药。在所有随后的 28 天周期中,维奈托克以目标剂量开始。对于随机分配到安慰剂组的患者,安慰剂(外观相同的片剂)以与 维奈托克相同的方式给药。
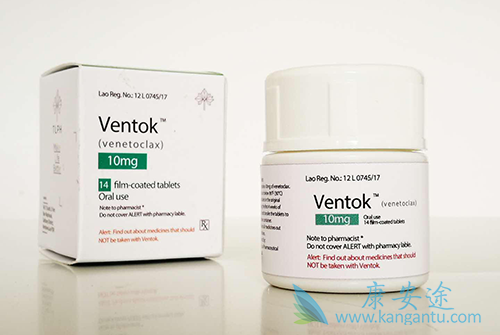
对于双臂患者,LDAC (20 mg/m2) 在所有周期的第 1 至 10 天通过皮下注射每天一次给药。患者可以继续接受治疗直至疾病进展或达到研究治疗终止标准。患者继续接受 OS 评估和随访研究,即使他们开始了额外的治疗。由于维奈托克是一种 CYP3A 和 P-糖蛋白 (P-gp) 底物,对接受这些抑制剂的患者应用了方案推荐的剂量修改:如果与中度 CYP3A 抑制剂或 P-gp 抑制剂共同给药,维奈托克剂量减至 50%,并减至如果与强 CYP3A 抑制剂共同给药,则为 50 mg。如果患者使用多种抑制剂,则根据最强的抑制剂调整维奈托克剂量。
总共有 211 名患者入组,210 名接受治疗;68 名患者随机分配至安慰剂组(安慰剂加 LDAC),143 名患者随机分配至维奈托克组(维奈托克加 LDAC;其中 1 名患者从未接受过治疗)。在维奈托克组(截至 2019 年 2 月 15 日),中位治疗持续时间为 3.9 个月(范围,0-17 个月),中位周期数为 4。在安慰剂组中,中位治疗持续时间为 1.7 个月(范围,0.1 -14 个月),治疗周期的中位数为 2。研究的中位数时间(无事件患者的观察时间)为 12 个月。
维奈托克加 LDAC 组 143 名患者中有 33 名 (23%) 接受了研究后治疗,安慰剂组 68 名患者中有 30 名 (44%) 接受了研究后治疗。没有患者在研究治疗后继续进行干细胞移植。停止研究药物(维奈托克加 LDAC 与安慰剂加 LDAC)的主要原因是:治疗失败(12% 对 19%)、疾病进展(11% 对 16%)、死亡(两者均为 12%)、撤销同意( 6% vs 10%)、与疾病进展无关的 AE(两者均为 9%)、与疾病进展相关的 AE(两者均为 4%)、医师决定(5% vs 12%)、形态学复发(13% vs 4%) ) 和其他(4% 对 3%)。
由治疗臂分开。在所有患者中,中位年龄为 76 岁,32% 的细胞遗传风险较差,38% 患有继发性 AML,20% 有既往 HMA 暴露史,19% 检测到TP53、FLT3、IDH1/2或NPM1 的基线突变,分别为 18%、20% 和 15% 的患者。大多数基线特征在随机组中具有相似的频率,除了继发性 AML 的发生率(41% 对 34%),后者在维奈托克组中更常见。现在维奈托克的价格是多少?更多详情可咨询下方微信。














请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)