肿瘤异质性加剧了去势抵抗性前列腺癌 (CRPC) 的难治性,包括雄激素受体 (AR) 轴的不同改变和 AR 非依赖性表型。包含这种异质性的其他模型的可用性将有助于确定更有效的 CRPC 疗法。在过去十年中,晚期前列腺癌的新全身治疗延长了患者的生存期,但也提出了新的临床挑战。转移性去势抵抗性前列腺癌 (CRPC) 由于抵抗机制,包括内分泌雄激素合成、AR基因的基因组改变(扩增、功能获得性突变和重排)、AR 剪接的表达,通常维持雄激素受体 (AR) 信号传导AR 辅因子表达或活性的变异和改变。因此,第二代 AR 导向抑制剂,如阿比特龙(abiraterone)或恩杂鲁胺,已经有效;然而,患者不可避免地会在这些药物上取得进展,并出现不同的耐药表型。
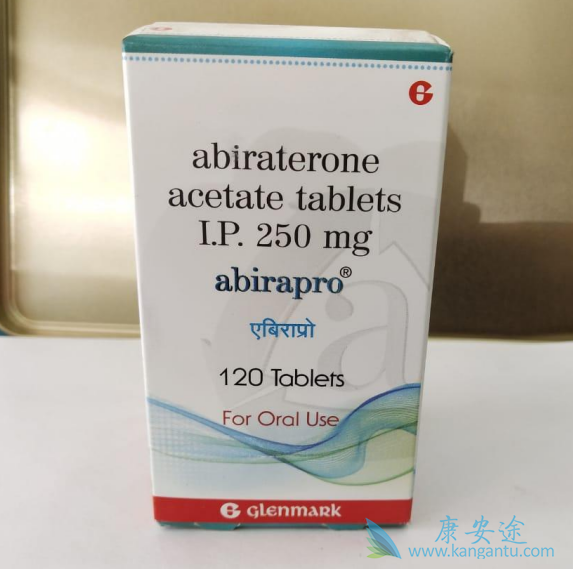
例如,肿瘤耐阿比特龙和恩杂鲁胺能够朝向过渡侵略性AR-空/ AR-独立的表型,包括小细胞和/或神经内分泌(NE)癌症和双阴性(AR空和NE空)前列腺癌。重要的是,这些临床和基因组特征的大量患者内部和患者间异质性使得开发新的治疗策略具有挑战性。在这项研究中,我们从对传统雄激素剥夺疗法、第二代 AR 导向抑制剂和化疗耐药的患者开发了当代 CRPC 的新型患者来源异种移植物 (PDX),具有广泛的耐药机制。我们使用这些 PDX 以及源自它们的外植体和类器官来测试候选疗法。
通过利用体现 CRPC 异质性的患者衍生模型来发现治疗策略。从两名患者的独立转移瘤中建立了四个新的患者来源的异种移植物 (PDX),并使用整合基因组学进行了表征。使用创新的离体 PDX 培养系统对一组合理选择的药物进行了测试。
评估了以下药物:AR 信号抑制剂(恩杂鲁胺和加列酮)、PARP 抑制剂(他拉唑帕尼)、化疗药物(顺铂)、CDK4/6 抑制剂(瑞博西尼)、溴结构域和末端 (BET) 蛋白抑制剂(iBET151 和 JQ1)和核糖体生物发生/功能抑制剂(RNA 聚合酶 I 抑制剂 CX-5461 和泛 PIM 激酶抑制剂 CX-6258)。
使用免疫组织化学对 Ki67 和裂解的 caspase-3 水平评估 PDX 组织离体培养物中的药物功效。还测试了候选药物的体内抗肿瘤功效,肿瘤体积是主要终点。双尾t检验用于比较药物治疗和对照治疗。综合基因组学表明,新的 PDX 表现出异质性的耐药机制,包括已知和新的AR突变、AR基因的基因组结构重排和神经内分泌样 AR 无效表型。尽管存在异质性,但所有模型都对核糖体靶向剂 CX-5461 和 CX-6258 的组合敏感。
这项研究表明,核糖体靶向药物可能对多种 CRPC 亚型(包括 AR 无效疾病)有效,并强调了当代患者衍生模型优先考虑临床转化治疗策略的潜力。现在阿比特龙的价格是多少?更多详情可咨询下方微信。












请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)