2015年6月启动了针对EGFR-wt,ALK-wt晚期NSCLC患者的II期单臂,多中心国际研究,该研究仍在进行中。在这项建议使用400毫克BID片剂的推荐剂量研究中,患者入组研究了谁将从卡马替尼(INC280)治疗中受益最大(例如MET外显子14跳过突变或MET扩增,包括GCN分层;一线或进一步治疗) ),并对每个队列分别进行分析。参加MET预处理人群在预先计划的中期分析之后,出于无用的目的,停止了<10 GCN的扩增。
ALK,间变性淋巴瘤激酶;EGFR,表皮生长因子受体;GCN,基因拷贝数;NSCLC,非小细胞肺癌。其余正在进行的队列为:METGCN≥10的预治疗患者队列1a;队列4与MET外显子14突变的预治疗患者相关,而与GCN无关;队列5与未治疗的MET失调患者(5a:METGCN≥10和5b:MET外显子14突变,与GCN无关);具有METGCN≥10而无MET外显子14突变或MET外显子14突变而与GCN无关的预治疗患者的第6组;队列和第7队列(扩展队列)与未接受过MET外显子14突变治疗的初治患者(无论MET如何)GCN。在此中期分析的截止日期(2018年11月8日),已完成MET突变队列4(n = 69)和5b(n = 28)的入组。
主要结局指标是ORR,它是根据RECIST 1.1通过盲独立审查委员会(BIRC)评估得出的CR或PR总体反应最佳的患者比例。次要结局指标包括反应持续时间(DOR [主要次要目标];根据RECIST 1.1通过BIRC评估首次记录CR或PR的日期,到因任何原因导致的第一个记录进展或死亡的时间计算得出PR或CR),通过研究者评估的ORR,DCR,无进展生存期(PFS)和总体生存期(OS;定义为从首次服用卡马替尼到因任何原因死亡的时间)。评估安全性结果并以发生AE和严重AE的患者人数表示。
队列4和5b的初步数据可用,这些数据已在2019年ASCO大会上发表。通过BIRC分析,第4组患者(MET外显子14突变的预治疗患者,无论GCN如何;第二/三线[2/3 L])的ORR达到39.1%。在进行此分析时,BOR的中值DOR仍不成熟,据报道为9.72个月。在队列5b中(未接受过MET治疗的患者不考虑GCN的突变;一线[1L]),ORR为71.4%。
DOR的中位数(通过BIRC)为8.41个月(在该截止日期也未成熟)。此外,队列4中的PFS中位数为5.42个月(2/3 L),队列5b中的PFS中位数为9.13个月(1L),但是队列5b的PFS结果在该分析的截止日期尚未成熟。在未接受治疗的患者和接受过治疗的患者之间观察到的不同收益凸显了需要对MET外显子14跳过突变晚期NSCLC的患者进行早期诊断。已知卡马替尼可穿越血脑屏障并在脑转移中显示出初步活性。队列4中的一名患者(无论是否患有GCN均经过MET突变治疗的预治疗患者)的病例报告显示,在基线基线后第一次CT扫描(卡马替尼治疗42天后),脑转移得以完全解决。
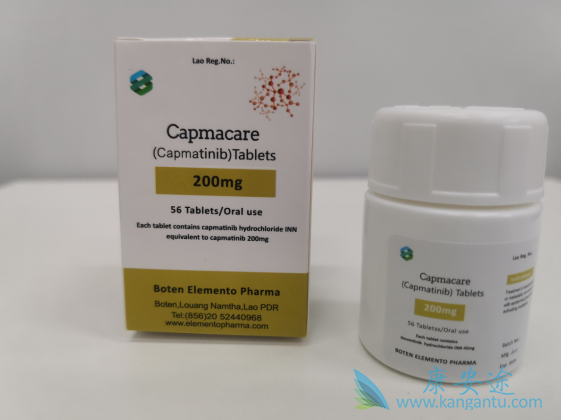
不论是否因果关系,所有队列(n = 315)中最常见的不良事件(≥25%)包括外周水肿(49.2%),恶心(43.2%)和呕吐(28.3%)。在这些队列中,卡马替尼在禁食条件下给药。但是,在扩展队列(队列6和7)中,卡马替尼的给药与喂食或禁食状态无关。现在还是非常推荐卡马替尼的购买的,更多详情可咨询下方微信。













请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)