I期研究(NCT01324479)已针对患有MET改变的实体瘤(包括NSCLC,n = 55)患者进行。这项研究旨在包含剂量递增(n = 38,无NSCLC)和剂量扩展部分,后者包括原始扩展组(n = 26 NSCLC)和附加扩展组(n = 29 NSCLC)。该研究的主要目的是确定最大耐受剂量/推荐的II期剂量(RP2D)以及卡马替尼(INC280)作为单一口服药物的安全性和耐受性。次要目标是疗效评估(在RP2D时具有完全缓解[CR]或部分缓解[PR]的患者的比例)和药代动力学(PKs)。
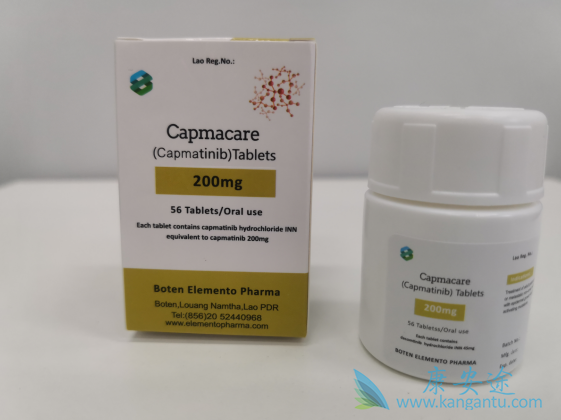
在剂量增加部分和原始扩展组中,患者的MET改变定义为MET / CEP7比≥2.0,或GCN≥5,或IHC H评分≥150。H评分是通过将染色强度乘以得到的(0至300之间)的IHC染色细胞百分比(0%至100%);因此,它的值介于0到300之间。而且,这些患者没有记录的EGFR状态。
该研究的剂量增加部分招募了38例实体瘤患者在7个剂量为100-600 mg每日两次(BID)胶囊或400 mg BID片剂的队列中进行治疗。剂量限制毒性发生在200 mg BID,250 mg BID和450 mg BID胶囊(每个1位患者)上,并达到3级疲劳(2位患者),并且3级血清胆红素升高。
任何级别的最常见药物相关不良事件(AE)为恶心(33%),疲劳(25%)和呕吐(24%),最常见的药物相关3/4 AE不良反应为疲劳(4 %)和增加的脂肪酶水平(3%)。卡马替尼的血浆浓度通常随剂量而增加,RP2D被确立为600 mg BID胶囊,但开发并测试了膜衣400 mg片剂以提高患者的便利性和依从性。值得注意的是,使用400 mg BID片剂的剂量具有可比的耐受性,安全性和暴露于600 mg BID胶囊的情况。
附加膨胀组中的患者已经集中评估MET状态如IHC 3+和记录EGFR野生型[重量]状态。在研究的剂量扩展部分中,截至2016年3月15日的分析截止日期,在55名晚期NSCLC患者中,有11名(20%)达到了PR,总缓解率(ORR)为20%疾病控制率(DCR; CR或PR或稳定疾病患者的比例)为51%。在可评估的患者与MET IHC3 +(不管GCN状态)ORR为24%,并且在患者的47%METGCN≥6。
这些结果表明,与IHC状态相比,FISH对MET状态的分析更好地预测了反应。当时,IHC被放弃作为卡马替尼活性的可能预测生物标志物。最常见的不良事件(所有级别,不论是否因果关系)为恶心(47%),周围水肿(38%),呕吐(36%),食欲下降(33%)和疲劳(29%)。最常见的严重不良事件是3级一般身体健康恶化(6%),3级腹痛,2级和3级肺炎,3级脱水和2级肺栓塞(均为4%)。在还是非常推荐卡马替尼的购买的,更多详情可咨询下方微信。














请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)