MET基因突变发生于百分之三到百分之四的非小细胞癌(NSCLC)患者中,这些患者一般的年纪相对来说大些 ,预后较差。MET基因突变既可以是驱动基因,又在导致其他驱动基因耐药方面扮演一个重要的角色。由于NSCLC的患者群体庞大,MET突变的患者数量也不容忽视。
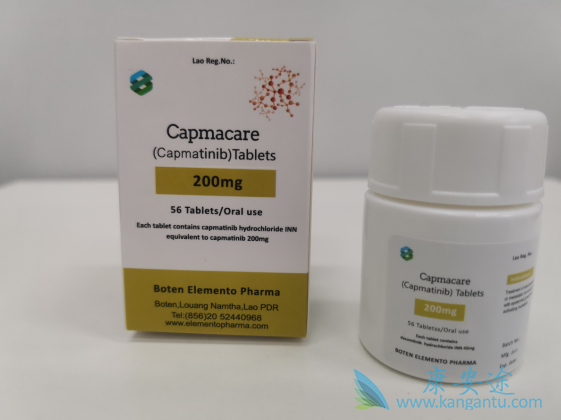
诺华(Novartis)公司宣布,美国FDA批准其MET抑制剂卡马替尼(Tabrecta,Capmatinib)上市,治疗携带MET基因外显子14跳跃突变的晚期非小细胞肺癌(NSCLC)患者。这些患者的基因突变需要经过FDA批准的检测确认。这是FDA批准的针对MET基因外显子14跳跃突变患者群的首款靶向疗法。
卡马替尼(Tabrecta,Capmatinib)是一种可以直接吃的高选择性小分子MET抑制剂,卡马替尼(Tabrecta,Capmatinib)最开始是由Incyte发现,诺华在2009年获得它的研发和推广许可。此前,FDA曾授予它突破性疗法认定和孤儿药资格,也对它的新药申请颁发了优先审评资格。
FDA的批准是因为一项GEOMETRY mono-1的2期临床试验,研究人员招募了97名带有MET外显子14跳跃突变的晚期或转移性NSCLC患者。研究结果表明,无论患者先前是否曾接受过治疗,卡马替尼(Tabrecta,Capmatinib)均能带来显著治疗效果。在初治和经治患者中,卡马替尼(Tabrecta,Capmatinib)的总缓解率分别为68%(95% CI: 48-84)和41%(95% CI: 29-53)。两组患者的中位缓解持续时间分别是11.14个月和9.72个月。
“非小细胞肺癌是一种复杂的疾病,很多不同的基因突变可能促进癌症的生长,”GEOMETRY研究负责人Juergen Wolf博士说:“MET基因外显子14跳跃是一种已知的癌症驱动因子。今天FDA的批准上市,让我们能够检测并且使用靶向疗法治疗这种具有挑战性的肺癌,为携带这类突变的NSCLC患者带来希望。”详情请扫码咨询:















请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)