与安慰剂组相比,索马鲁肽(司美格鲁肽)组的胃肠道疾病更常见。大多数胃肠道事件的严重程度为轻度或中度,发生在前 30 周。与安慰剂组相比,索马鲁肽组因不良事件(主要是胃肠道)而中断治疗的频率更高。索马鲁肽组严重不良事件(包括严重心脏疾病)的频率和发生率低于安慰剂组。
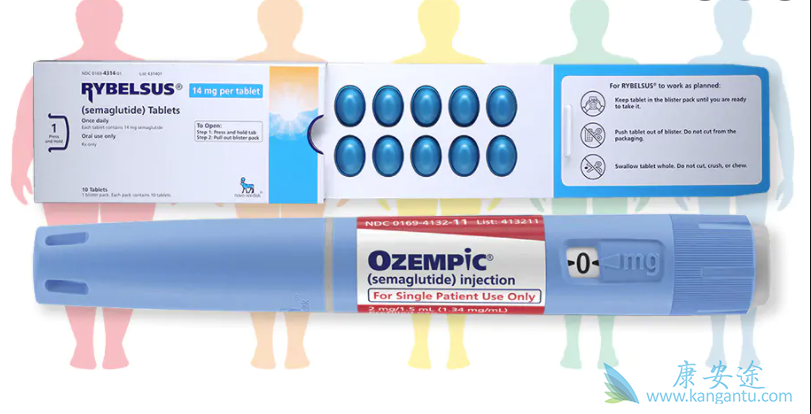
索马鲁肽组 9 例患者发生急性胰腺炎,安慰剂组 12 例患者发生急性胰腺炎;根据修订后的亚特兰大标准,所有事件都是轻微的。索马鲁肽组的脂肪酶和淀粉酶水平显着高于安慰剂组。索马鲁肽组 58 名患者和安慰剂组 61 名患者发生胆囊疾病。两组的恶性肿瘤发生率相似,与安慰剂组相比,索马鲁肽1.0 mg 组较高,0.5 mg 组较低。1 名接受 1.0 毫克司美鲁肽的患者和 4 名接受安慰剂的患者发生了胰腺癌。在任一治疗组中,事件裁定委员会均未确认甲状腺髓样癌。在接受司美鲁肽治疗的 30 名患者中检测到抗司美鲁肽抗体,其中最多的患者 (14) 在第 44 周检测为阳性。在大多数患者中,抗体形成是短暂的――只有 4 名患者在随访期间检测为阳性――并且抗体滴度普遍较低。
与安慰剂剂量的索马鲁肽相比,0.5 mg 和 1.0 mg 剂量的司美鲁肽(分别为 191 [23.1%] 和 178 [21.7%])观察到类似的严重低血糖发作或低血糖的发生率和发生率0.5 和 1.0 毫克(177 [21.5%] 和 173 [21.0%])。在这项心血管结局试验中,我们证实了我们的主要假设,即索马鲁肽不劣于安慰剂。与接受安慰剂的患者相比,接受司马鲁肽治疗的患者发生心血管原因死亡、非致死性心肌梗死或非致死性中风的主要复合结局风险显着降低 26%。这种较低的风险主要是由于非致命性卒中发生率显着 (39%) 下降和非致命性心肌梗死发生率不显着 (26%) 下降,心血管死亡率没有显着差异。两种剂量的司美鲁肽均观察到类似的风险降低。根据 Kaplan-Meier 估计,在 24 个月内需要接受治疗以预防主要结局事件的患者人数为 45。大多数研究患者在基线时接受心血管风险管理,如接受抗高血压、降脂和抗血小板药物治疗的患者比例很高。尽管脉搏率增加,但主要结果的风险降低,这是 GLP-1 受体激动剂的类效应。
根据大量白蛋白尿的差异,接受索马鲁肽治疗的患者发生新肾病或恶化肾病的风险较低,但与接受安慰剂的患者相比,发生糖尿病视网膜病变并发症的风险较高。尽管视网膜病变事件的总数较低,但在司美鲁肽组中,视网膜病变并发症(玻璃体出血、失明或需要玻璃体内药物或光凝治疗)的发生率出乎意料地更高。据报道,在 1 型糖尿病患者中,快速降糖与视网膜病变恶化之间存在关联。这种关联对我们发现的适用性尚不清楚,不能排除司美鲁肽的直接影响。
与安慰剂相比,索马鲁肽与糖化血红蛋白水平显着和持续降低相关,低血糖发生率相似。在试验期间,与司美鲁肽组相比,安慰剂组中更多的患者加强了他们的抗高血糖治疗。然而,糖化血红蛋白水平的组间差异在 2 年后仍然存在。与安慰剂组相比,索马鲁肽组在 2 年内出现了具有临床意义且持续的体重减轻和收缩压降低。糖化血红蛋白、体重和收缩压的降低可能都有助于观察到使用司美鲁肽降低心血管风险。
除视网膜病变并发症外,司美鲁肽的安全性与其他 GLP-1 受体激动剂相似。合并司美鲁肽组和合并安慰剂组的恶性肿瘤发生率相似,尽管在 1.0 mg 司马鲁肽剂量下观察到的发生率最高。索马鲁肽的胰腺癌发生率(该药物类别的一个重要事件)较低,并且在该试验中没有报告甲状腺髓样癌。两个合并组中发生胰腺炎的患者数量虽少但相似。
迄今为止,两种降糖药已被证明可以降低心血管风险高的 2 型糖尿病患者的心血管事件发生率。2,3在该试验中,主要结果的风险降低是由非致命性卒中发生率的显着下降和非致命性心肌梗死发生率的非显着下降驱动的,心血管死亡没有差异。司美鲁肽对心血管结局的有益作用可能与改变动脉粥样硬化的进展有关。
该试验是一项非劣效性研究,排除了食品和药物管理局设定的 1.8 的批准前安全边际。它没有能力表现出优越性,因此没有预先指定此类测试。然而,司美鲁肽的治疗效果和超过事件的计提估计造成的主要成果的患者在司美鲁组之间的显著降低风险。术后随访持续时间相对较短(2.1岁),均在高心血管风险。这些研究结果对其他人群的普遍性和治疗持续时间较长的是未知的。这也是不明就里促成的结果司美鲁群什么程度更大的糖化血红蛋白降低。总之,病人型中2型糖尿病患者在高心血管风险,死亡的第一次出现心血管原因,非致死性心肌梗死,或非致死性卒中的发生率为显著那些接受司美鲁低于那些接受安慰剂,这证实非劣效性。索马鲁肽更多信息可咨询下方微信。














请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)