美国食品和药物管理局(FDA)今天扩大了艾伯维公司Mavyret(格卡瑞韦/哌仑他韦)片剂的批准范围,可用于对患有全部基因型(基因型G1-6)的慢性丙肝病毒(HCV)感染、代偿性肝硬化和未接受过HCV治疗的儿童(12岁及以上或体重不低于99磅)和成人患者,治疗疗程为八周。目前,Mavyret是第一个八周治疗丙肝的方法。在这之前,代偿性肝硬化患者的标准治疗期限为十二周,甚至更长时间。
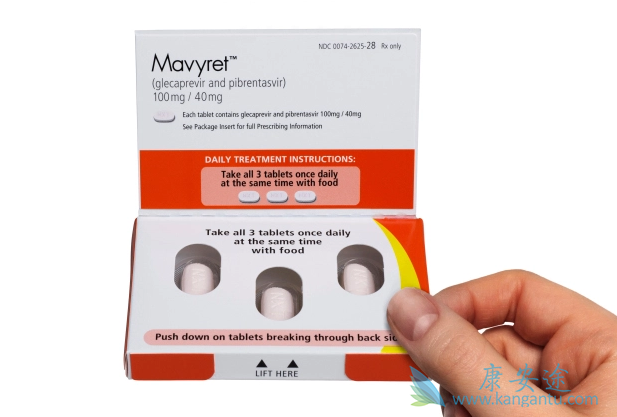
这项批准为患有代偿性肝硬化的成人和儿童患者提供了八周的治疗方案,并且不需要考虑HCV的基因型。Mavyret是一种复方药物,可通过抑制病毒繁殖将体内HCV降低至无法检测的水平,大多数情况下可治愈HCV感染。HCV是一种病毒性疾病,会引起肝脏炎症,从而导致肝功能减弱或肝功能衰竭。
临床试验显示了Mavyret的有效性和安全性。该试验累计评估了2500例基因型1、2、3、4、5或6感染的HCV患者,分别接受Mavyret 8、12或16周的治疗。参与试验包括HIV合并感染、肾或肝移植受者以及晚期肾脏疾病的患者(包括需要血液透析的患者)。在整个临床试验中,Mavyret的SVR 12在91-100%之间。
详情请访问 丙肝 http://www.kangantu.org/hcv/









请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)