剂量发现研究评估了乐伐替尼,一种口服多靶点受体酪氨酸激酶抑制剂,与卡铂/紫杉醇联合用于新化疗的非小细胞肺癌(NSCLC)患者。
患者和方法:
患者接受乐伐替尼每天2次(BID),卡铂(曲线下面积6mgml-1分钟-1,第1天)/紫杉醇(200mgm-2,第1天)每3周。乐伐替尼初始剂量为6mgBID。主要终点为乐伐替尼的最大耐受剂量(MTD)。在MTD阶段,队列扩大了16名患者。评价其安全性、药代动力学、药效学和抗肿瘤作用。
结果:
其中28例接受了治疗。在6mgBID,限剂量毒性(dlt)包括发热中性粒细胞减少/牙龈感染(n=2)。4mgBID时未发生dlt,推荐MTD扩大。常见的3/4级毒性反应包括中性粒细胞减少、白细胞减少、高血压和血小板减少。联合用药对单个药物的药代动力学无显著影响。有效率为68%,中位无进展生存期为9.0个月,4mgBID。在血浆生物标志物分析中,基质细胞衍生因子1α、干细胞因子和粒细胞集落刺激因子与抗肿瘤活性相关。
结论:
乐伐替尼联合卡铂/紫杉醇治疗晚期NSCLC患者的MTD为4mgBID。该方案具有可控的耐受性和鼓励抗肿瘤活性。
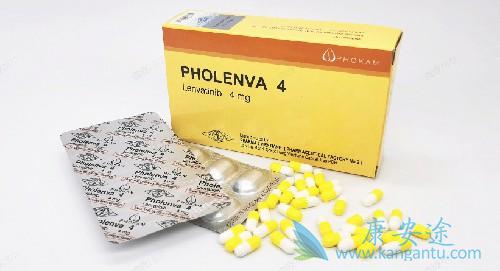
本研究的主要目的是通过乐伐替尼与卡铂/紫杉醇联合每日两次口服DLTs的发生率来确定晚期NSCLC患者的MTD。乐伐替尼起始剂量为6mgBID。2/6的患者出现dlt,即发热性中性粒细胞减少和牙龈感染。在随后的入组中,当乐伐替尼剂量降低到4mgBID时,未观察到dlt。卡铂或紫杉醇联合较高剂量的乐伐替尼的适当减量在本研究中没有确定。
22例接受乐伐替尼4mgBID治疗的患者中,最常见的3级或4级血液毒性是中性粒细胞减少、白细胞减少、血小板减少和发热性中性粒细胞减少。AE数据与之前报道的接受卡铂/紫杉醇联合治疗的日本NSCLC患者的AE数据相似。但本研究中4级中性粒细胞减少、3级或4级血小板减少的发生率略高于上述研究。卡铂/紫杉醇联合cediranib(另一种VEGFR抑制剂)与卡铂/紫杉醇单独治疗相比,晚期NSCLC患者出现3级或4级中性粒细胞减少、血小板减少和发热性中性粒细胞减少的发生率更高。
此前一项关于乐伐替尼在日本实体瘤患者中的一期研究报告称,在其他DLTs中存在血小板减少(Yamada等,2011年)。这些结果表明,卡铂/紫杉醇联合乐伐替尼治疗导致的中性粒细胞减少和血小板减少可能会轻微增加。17例患者(77%)使用G-CSF,中性粒细胞减少得到了很好的管理,血小板减少通常通过中断剂量而不输血来控制。
在本研究中,最常见的非血友病毒性是高血压,乐伐替尼单药治疗已报道。高血压一般采用抗高血压药物治疗,未观察到4级高血压。本研究未报道与联合治疗相关的意外毒性的安全性问题。然而,该结果表明,非小细胞肺癌患者联合使用乐伐替尼和卡铂/紫杉醇时,应监测其血液毒性的潜在增加。
该研究结果显示,在MTD为4mgBID时,其抗肿瘤活性为68%,中位PFS为9.0个月。因此,乐伐替尼4mgBID是与卡铂/紫杉醇联合治疗非小细胞肺癌进一步研究的推荐剂量。然而,该组合的乐伐替尼剂量低于乐伐替尼单药治疗的MTD,MTD为10mgBID。
目前研究中的药代动力学分析表明,乐伐替尼暴露联合卡铂和紫杉醇治疗晚期实体瘤患者与乐伐替尼单药治疗观察到的相似。在乐伐替尼的4和6mgBID剂量中,卡铂和紫杉醇的估计药代动力学参数基本一致,与历史数据相似。总的来说,这些结果表明,在本治疗方案中,乐伐替尼、卡铂和紫杉醇联合用药对这三种药物的药代动力学没有显著影响。
本研究中观察到相对较高的ORR和较长的PFS。NSCLC的发病机制和进展可能涉及VEGF通路抑制后出现的多种收敛和代偿生长因子信号通路,这可能解释了对VEGF靶向治疗的固有或获得性耐药性。多变量分析的335个病人经历了切除肿瘤样本阶段I-IIIANSCLC发现A的高表达与淋巴结转移相关,而高co-expressionPDGF-B和VEGFR3是一个强大和独立的预测差非小细胞肺癌患者的生存期。
异常的fgfr介导的信号传导、多态性以及FGFR1和FGFR2表达的增加也与NSCLC的发病机制和进展有关。其他临床前证据表明PDGFR和fgfr介导的信号通路可能协同促进肿瘤血管生成和转移。因此,通过靶向vegf、FGFRs和PDFGRs,乐伐替尼有可能抑制参与肿瘤血管生成的多个信号通路。
生物标志物分析在识别几种癌症治疗的潜在反应方面变得越来越重要。然而,迄今为止,对于具有预后或预测相关性的抗血管生成治疗,需要验证的生物标志物。血浆血管生成蛋白和细胞因子可能是有效的预测抗血管生成治疗反应和耐药性的指标。一些骨髓来源的细胞群通过不同的过程促进或抑制肿瘤的进展。这些细胞包括循环内皮祖细胞(CEP)、Gr1+和CD11b+骨髓源性抑制细胞以及VEGFR-1+血管细胞。SDF1α,SCF和G-CSF可能在招募这些细胞到血管生成位点上发挥作用,从而有助于化疗和抗血管生成治疗的耐药性。
在一项针对晚期实体瘤患者的乐伐替尼一期研究中,较低剂量前SDF1α水平与较长的治疗时间相关。同样,目前的研究表明,较低的剂量前SDF1α水平与更大的肿瘤收缩和更长的PFS显著相关。因此,较高的剂量前SDF1α水平可能预示着NSCLC患者对乐伐替尼治疗的耐药性。此外,治疗相关的G-CSF增加与较短的PFS相关。
粒细胞集落刺激因子的增加可能由于紫杉醇诱导的G-CSF增加CEP积累而促进对乐伐替尼(仑伐替尼)组合的耐药性。相比之下,治疗相关的SDF1α和SCF升高的患者分别有更长的PFS和更大的肿瘤收缩。尽管这些因素在肿瘤组织中的功能仍有待阐明,但在治疗过程中监测血浆中的这些因素可能是一种潜在的方法,可以识别预测该联合治疗方案的临床活性的生物标志物。详情请扫码咨询:













请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)