葛兰素史克(GSK)向中国媒体确认,希瑞适(Cervarix,人乳头状瘤病毒疫苗16型和18型)获得国家食药监总局的批准,成为国内首个获批用于预防宫颈癌的HPV疫苗,有望在明年年初正式上市。
尽管目前HPV疫苗已被全球160多个国家和地区批准使用,但是,在中国内地却迟迟未能上市,最大原因是,由于安全性存在争议,宫颈癌疫苗之前未被中国国家食药监总局批准,因此才会有10多年的迟滞。
HPV病毒与子宫颈癌
HPV病毒(人乳头瘤病毒的英文缩写)是一种属于乳多空病毒科的乳头瘤空泡病毒A属,是球形DNA病毒,能引起人体皮肤黏膜的鳞状上皮增殖.已分离出130多种,该病毒只侵犯人类,性传播是其感染的主要渠道,在18至24岁且未经性生活的女性群体中,“感染该病毒的可能性很低。”
一旦感染HPV病毒造成的后果是多年不能痊愈,该病毒会造成感染处皮肤像长了红色、污灰色的烂菜花瓣状,而且患处容易出血,使患者身心受到极大折磨。
据不完全统计,每年全世界有50万的女性因感染HPV病毒而患宫颈癌,其中20万死于该肿瘤,HPV病毒与艾滋病、癌症一起世界卫生组织列为人类三大绝症。
2015中国癌症统计报告显示,在女性特有的肿瘤中,宫颈癌位居第二,仅次于乳腺癌,是最常见的妇科恶性肿瘤,且发病年龄日益年轻化,据资料,目前,宫颈癌平均发病年龄由20年前的54岁,提前到45岁。
2015年国内宫颈癌新发病例估计9.89万例,死亡人数3.05万例,城市高于农村,考虑到缺乏筛查和治疗的人群,实际患者数应高于统计数据。
HPV疫苗的作用HPV疫苗,是预防HPV病毒(人类乳头瘤病毒)的疫苗。疫苗接种后,可刺激免疫系统产生保护性抗体,这种抗体存在于人的体液之中,HPV病毒一旦出现,抗体会立即作用,将其清除,阻止HPV病毒感染,,从而达到预防HPV感染的目的。而HPV病毒感染被发现是导致宫颈癌和生殖器湿疣以及部分肛门癌、口腔癌的主要因素。

因此,HPV疫苗很多时候又被人们习惯性称为子宫颈癌疫苗,这种说法虽然不规范,但也表明了HPV疫苗对预防子宫颈癌的巨大作用。
但是,现有的HPV疫苗无法针对所有类型的HPV病毒,只能抵抗最有可能引发宫颈癌的病毒类型,注射疫苗后可以降低患宫颈癌的几率,但并不能100%预防宫颈癌。
澳门卫生局强调,虽然疫苗可预防约七成的宫颈癌,但仍有三成宫颈癌可由不能被疫苗预防的其他高危型HPV病毒引起,而且疫苗不能治疗已受感染人士体内的病毒。
超一百个国家上市HPV疫苗 香港已引进十年
2006 年,世界上第一支可以预防癌症的疫苗——HPV疫苗,由美国食品药品监督管理局(FDA)批准上市,并获得世界卫生组织(WHO)的认可。早在2014年,WHO就发布指南,呼吁大家接种宫颈癌疫苗,认为接种宫颈癌疫苗和定期进行宫颈筛查,是最有效的防控措施。
在随后的7年间,100个多国家应用HPV疫苗,大幅降低HPV患病率和癌前病变发生率。截止目前,HPV疫苗已被全球160多个国家和地区批准使用。
根据公开报道发现,早在十年前, HPV疫苗就已获准在香港上市。根据香港药剂师学会的资料显示,自2006年11月至2014年,只有约8.85%的女性接种,其中还包括未必打足全套3针、非香港永久居民等情况。
内地女性热衷于赴港接种
虽然从2007年HPV疫苗就开始了中国内地的上市之路,但由于新药审评标准存在争议,它依然是被禁止的。
由于宫颈癌疫苗HPV最近几年在社交媒体上成讨论热点。在网络搜索引擎输入“HPV 疫苗 攻略”,不乏赴香港的接种帖子或例子。过去几年,组织内地人前往香港接种HPV疫苗已经形成了一个成熟完整的产业。
据了解,由于该疫苗共3针,需于6个月内分3次肌肉注射,也就意味着接在半年内,接种者需为特意从内地飞至香港注射。
《东方早报》报道中称,据曾去香港打HPV疫苗的毛女士介绍,打疫苗前需要进行一次妇科体检,证明并未患有感染HPV病毒,共需注射3针。
她称,“首次注射后2个月才可以注射第二针,第三针需要在首次注射后6个月才可以注射。”这意味着她在半年内要去3次香港,其中花费的成本和时间、精力均也不少。
另外,她透露,一度想在上海接种HPV疫苗,但从一些外资医院了解到,3针的价格是香港的近3倍,才决定去香港打。
内地苦等十年才盼来HPV疫苗
宫颈癌疫苗有望在明年上市的消息,让很多人兴奋不已。对于女性来说,这无疑是一项福利。
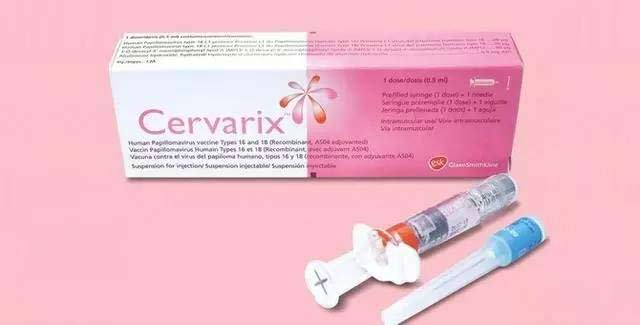
HPV疫苗"希瑞适"
尽管HPV疫苗在全球100多个国家和地区得到推行,但在长达十年的时间内,在我国内地,这片区域长期处在空白。有学者研究显示,2006-2012 年间,因为9到15岁的女孩未能接种HPV疫苗,可能造成中国未来38万的宫颈癌新发病例和21万宫颈癌死亡病例。
据了解,HPV迟迟未能上市的最大原因是,由于安全性存在争议,宫颈癌疫苗之前未被中国国家食药监总局批准,因此才会有10多年的迟滞。
按照我国现行规定,所有进口疫苗被批准在国内上市以前,必须在国内重新开展临床试验。疫苗临床试验结束后,由国家食品药品监督管理总局药品评审中心组织专家对其进行评审。符合规定者,发给《进口药品注册证》,准许进口。评审的时间根据药物的区别而不同,会持续1-5年不等。
这牵涉到一个极为关键的问题——什么是判断疫苗有效性的终点指标?
在我国FDA的标准里,疫苗有效性的评价终点是发生癌症或者出现宫颈上皮内2级以上瘤变。
那么出于伦理学等方面的考虑,一个疫苗在做大规模试验时,会选择以2级以上的癌前病变和HPV持续感染为复合终点,但这也需要数万人和不同地区参与,才能得出有价值的结果,这意味着临床试验的过程将非常漫长。
2014年,WHO发布了《预防HPV疫苗实验的主要重点专家小组报告》,其中提到,真正判断疫苗有效性的种地那其实是癌症指标,但将其作为有效性结果太不切实际——这不仅需要巨大的实验群体和财力支持,并很有可能得到并不显著的结果。
报道建议,将宫颈或肛门内6个月或更长时间的HPV持续感染,作为临床试验的提到终点指标来评估疫苗的有效性。
另外,有关专家分析,HPV病毒分型非常复杂,中国人感染的亚型主要是HPV16和HPV18,而欧美国家人主要感染的是HPV52、HPV58等,因此西方国家的疫苗不能拿来就用,必须针对中国的情况开发疫苗,且要经过长时间的安全、有效性试验后,才能引入市场。
(责任编辑:康安途海外医疗)







